Skånsom kræftbehandling med nanopartikler virker
Kræftbehandling baseret på bittesmå nanopartikler, som sprøjtes direkte ind i kræftknuden virker, og kan ødelægge kræften indefra. Forskere fra Niels Bohr Institutet og Det Sundhedsvidenskabelige Fakultet på Københavns Universitet har udviklet en metode, som dræber kræftceller ved hjælp af nanopartikler og laserlys. Behandlingen er afprøvet på mus og viser, at kræftknuderne beskadiges betydeligt. Resultaterne er publiceret i det videnskabelige tidsskrift, Scientific Reports.
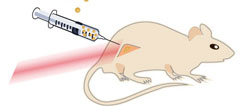
På tegningen ses en mus med en kræftsvulst på bagbenet. Nanopartiklerne sprøjtes direkte ind i kræftsvulsten, som derefter belyses med nær-infrarødt laserlys. Nær-infrarødt laserlys trænger fint igennem væv og giver ingen brandskader. (Credit: Kamilla Nørregaard, Panum Inst.)
Traditionelle kræftbehandlinger som strålebehandling og kemoterapi har store bivirkninger, da de ikke kun rammer kræfttumorerne, men også påvirker kroppens raske dele.
Et stort tværfagligt forskningsprojekt mellem fysikere på Niels Bohr Institutet samt læger og humanbiologer på Panum Instituttet og Rigshospitalet har udviklet en ny behandling, der kun rammer kræfttumorerne lokalt og derfor er meget mere skånsom for kroppen.
Projektet hedder Laser Activated Nanoparticles for Tumor Elimination (LANTERN). Leder af projektet er professor Lene Oddershede, der er biofysiker og leder af forskningsgruppen, Optisk Pincet på Niels Bohr Institutet ved Københavns Universitet i samarbejde med professor Andreas Kjær, leder af Cluster for Molecular Imaging, Panum Instituttet.
Efter eksperimenter med biologiske membraner har forskerne nu afprøvet metoden på levende mus. I forsøgene har musene fået kræfttumorer af laboratoriedyrkede menneskekræftceller.
”Behandlingen går ud på at sprøjte bittesmå nanopartikler direkte ind i kræftknuden. Derefter lyser man udefra på nanopartiklerne med laserlys. Der er en stærk vekselvirkning mellem nanopartiklerne og laserlyset, som bevirker, at partiklerne opvarmes. Der sker så det, at de opvarmede partikler beskadiger eller dræber kræftcellerne”, fortæller Lene Oddershede.
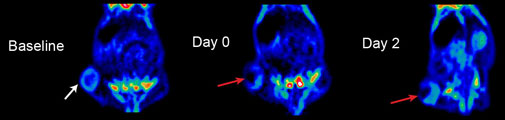
Billederne viser PET-scanninger af en mus med en stor tumor (ved den hvide pil). Tumoren behandles med nanopartikler, som sprøjtes direkte ind i tumoren og derefter belyses med nær.infrarødt laserlys. Laserlyset opvarmer nanopartiklerne, som dermed beskadiger eller dræber kræftcellerne (røde pile). (Credit: Kamilla Nørregaard og Jesper Tranekjær Jørgensen, Panum Inst.)
Design og virkning
De små nanopartikler er mellem 80 og 150 nanometer i diameter (en nanometer er en milliontedel af en millimeter). De testede partikler består enten af massivt guld eller en skal-struktur bestående af en glas-kerne med en tynd skal af guld omkring. En del af forsøgene har haft til formål at finde ud af, hvilke partikler, der er mest effektive til at mindske tumorer.
”Som fysikere har vi stor ekspertise i vekselvirkningen mellem lys og nanopartikler, og vi kan meget præcist måle temperaturen af de opvarmede nanopartikler. Virkningen afhænger af den rigtige kombination mellem partiklernes struktur og materiale, deres fysiske størrelse og lysets bølgelængde”, fortæller Lene Oddershede.

Forsøgene blev udført med nanopartikler af forskellig struktur og størrelse. De to første i rækken bestod af massivt guld, og den sidste bestod af en kerne af glas med en overflade af guld. Kuglerne blev belyst med nær-infrarødt lys med bølgelængder på henholdsvis 807 nanometer og 1064 nanometer. Det mest effektive nanopartikel var den guldbelagte glaskugle. (Credit: Kamilla Nørregaard, Panum Inst.)
Forsøgene viste, at forskerne fik de bedste resultater med nanopartikler, som var 150 nanometer i størrelse og bestod af en kerne af glas belagt med guld. Nanopartiklerne blev belyst med nær-infrarødt laserlys, som trænger bedst igennem væv. Modsat almindelig strålebehandling giver det nær-infrarøde laserlys ingen brandskader på det væv, det passerer igennem. Med PET-scanninger kunne de allerede en time efter behandlingen direkte se, at kræftcellerne blev slået ihjel, og effekten fortsatte i mindst to dage efter behandlingen.
”Nu har vi bevist, at metoden virker. På længere sigt vil vi gerne have metoden til at virke ved, at nanopartiklerne bliver sprøjtet ind i blodbanen, hvor de ender i kræftknuder, som kan have spredt sig i kroppen. Med PET-scanninger kan vi så både se, hvor knuderne befinder sig og belyse dem med laserlys, men også effektivt vurdere, hvorvidt behandlingen har virket kort tid efter bestrålingen. Derudover vil vi belægge partiklerne med kemoterapi, som frigøres af varmen, og som også vil medvirke til at slå kræftcellerne ihjel”, fortæller Lene Oddershede.

Lene Broeng Oddershede, professor, leder af Grundforskningscentret, StemPhys, leder af forskningsgruppen Optisk Pincet på Niels Bohr Institutet, Københavns Universitet, Tlf. +45 2494-2534, Email: oddershede@nbi.dk
Andreas Kjær, professor, leder af Cluster for Molecular Imaging, Panum Instituttet, Københavns Universitet, +45 3532-7504, akjaer@sund.ku.dk
