Radioaktivitet og spontane henfald
Hej Spørg om Fysik
Jeg kunne godt tænke mig at vide, hvad radioaktivitet er? Og Hvad spontane henfald er?
Med venlig hilsen
KK

Vi kender 92 grundstoffer i naturen, og noget over 100 grundstoffer når vi tager de stoffer med, der er frembragt i laboratoriet. De er bygget ensartet op. I midten sidder en atomkerne opbygget af protoner og neutroner. Udenom kredser et antal elektroner.
[Der er lidt flere stoffer. I Gabon i Afrika findes en naturlig atomreaktor dvs. et uranleje, hvor de processer der foregår i atomreaktorer har foregået i millioner af år, og hvor en række reaktorprodukter med højere nummer end nr. 92 forekommer].
Billedet er taget fra M. Brydensholt m.fl. Orbit 1, systime forlag.
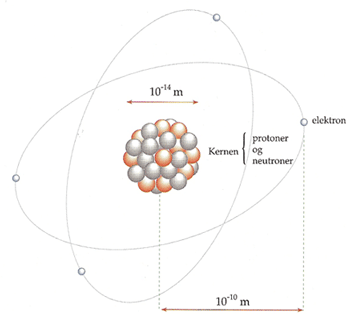 Selve kernen har en diameter omkring 10-14 m eller 0,000 000 000 01 m.m.
Selve kernen har en diameter omkring 10-14 m eller 0,000 000 000 01 m.m.
Atomet med elektronerne udenom ligger i en størrelse omkring 10-10 m eller 10 000 gange større end kernen altså 0,000 000 1 mm. Der er altså tale om noget meget småt.
Neutronen vejer omkring 1,6750*10-27 kg, protonen omkring 1,6726*10-27 kg, og elektronen 9,1095*10-31 kg.
Neutronen har ingen ladning, protonen har en positiv ladning som i en enhed som hedder Coulomb, man måler ladning i, er +1,6021773*10-19 C, elektronens ladning har samme størrelse, den er bare i stedet negativ ladet.
En kerne består af et antal protoner, fra 1 til ca. 100, og et nogenlunde tilsvarende antal neutroner. Kernen holdes sammen af kernekræfter, som virker fra partikel til partikel. Ladningerne i protonerne frastøder hinanden, men kernekræfterne er meget store, og holder dem sammen. Det er kræfter vi slet ikke opdager i dagligdagen, idet de er meget kortrækkende, og kun virker indenfor afstande, som svarer til kernernes størrelser.
Det der bestemmer hvilket stof kernen repræsenterer, er ladningen, dvs. antallet af protoner. Atomerne er normalt uladede, idet der for hver proton i kernen er en elektron udenom kernen, og da disses ladninger er lige store, med modsatte fortegn, bliver ladningen set udefra præcis 0. Atomernes normale fysiske og kemiske egenskaber bestemmes af elektronerne udenom kernen. Det er i særlig grad for de fleste stoffer de yderste elektroner (op til 7), som er bestemmende for disse egenskaber.
Henfald og ioniserende stråling
Nu har naturen det ikke altid med at gøre tingene enkle. Nok bestemmes kernens ladning af antal protoner, og der er et nogenlunde tilsvarende antal neutroner, men neutrontallet kan variere for et givet antal protoner. Man får så en kerne af samme stof, men måske lidt tungere. Der er oftest overskud af neutroner. Disse ens grundstoffer, med forskelligt neutrontal, kaldes isotoper. Bliver forholdet imellem neutroner og protoner ekstremt, har man en ustabil kerne, som henfalder ved det man kalder ioniserende stråling. Der er store forskelle på, hvor mange isotoper der findes i naturen, svarende til de forskellige grundstoffer.
For Brint (Hydrogen) findes der tre:
- Den almindelige brint med 1 proton .
- Tung brint (Deuterium) med en proton og 1 neutroner.
- Og endelig Tritium med 1 proton og 2 neutroner.
Tritium er ustabilt og derfor radioaktivt, og udsender det man kalder beta-stråling, og bliver så til Helium, herom nedenfor. Helium har tilsvarende 4 isotoper heraf 2 i naturen. Af gassen Krypton kendes 19 isotoper, af Tin kendes 20 isotoper heraf 10 i naturligt Tin. Af Jod kendes 19 isotoper heraf kun 1 i naturen.
Tre naturlige typer af stråling
- Alfa-stråling, hvor atomkernen udsender en Helium kerne. Derved ændres den oprindelige kerne til en ny (et andet stof), som ligger 2 trin længere nede i protontal.
- Betastråling, hvor kernen udsender en elektron og kernen så omdannes til et andet stof med en kerneladning en større. Disse to processer kan opfylde guldmagerens drøm, nemlig at omdanne andre stoffer til guld. Det er desværre meget dyrere at skaffe sig guld i laboratoriet på den måde, så vejen går stadig via guldsmeden.
- Endelig gammastråling som er elektromagnetiske stråling svarende til røntgen, lys og radiobølger, blot med højere energi og kortere bølgelængde. Atomet er her uændret, men har afgivet noget overskudsenergi (ofte efterladt af et tidligere henfald).
Der findes andre henfald, som især forekommer, på de isotoper vi selv har skabt i atomreaktorer eller acceleratorer. Alfa-strålingen ioniserer omgivelserne, f.eks. luften kraftigt, og bremses derfor hurtigt. Alfastråling stoppes i luft normalt indenfor ca. 3-5 cm (afhængigt af den energi dvs. fart de udsendes med).
 På billedet vises et "Tågekammerbillede" af alfa-spor. Bemærk, at de er lige lange fra præparatet (fra nettet). Alfastråling stoppes stort set i vores overhud, eller et stykke alu-folie fra køkkenet. Hvis vi rammes, og da det er døde celler, volder den som oftest ingen skader.
På billedet vises et "Tågekammerbillede" af alfa-spor. Bemærk, at de er lige lange fra præparatet (fra nettet). Alfastråling stoppes stort set i vores overhud, eller et stykke alu-folie fra køkkenet. Hvis vi rammes, og da det er døde celler, volder den som oftest ingen skader.
Optages alfa-strålende atomer i organismen (spises eller indåndes), volder de derimod alvorlige skader i deres nærhed. Betastråling udsendes fra kernen sammen med en anden uladet partikel, der hedder antineutrinoen. Det er en lidt spøgelsesagtig, og næsten masseløs partikel, som kun vekselvirker lidt med stof, og som let kan gå tværs igennem jorden uden at blive stoppet. Den volder derfor ikke skader på os.
Da de to partikler deler den energi der er til henfaldet, betyder det, at beta-partikler har rækkevidder i luft fra 0 cm, og op til omkring 20 m. Nogen af dem vil i mange trænge ind i de levende væv igennem huden, hvis vi bestråles, og giver skader. Som med alfa-partikler er de også yderst skadelige, hvis de optages i organismen.
Gamma-stråling er elektromagnetisk stråling med højere energi end røntgenstråling og UV eller synligt lys. For gammastråling taler men om en halveringstykkelse, dvs. den tykkelse stof hvor halvdelen af gammastrålingen stoppes i stoffet. For vand som ligner os mest, er halveringstykkelsen for mange forekommende gammastrålinger fra få cm til ca. 30 cm (efter 60 cm er der ¼ tilbage osv.), dvs. en sådan stråling vil normalt blive delvis stoppet i kroppen og gøre skade, ligesom gammastrålende atomer inde i kroppen gør skade.
I den nederste ende af det periodiske system, de atomer med lille nummer, sker naturlige henfald normalt ved, at en neutron udsender en elektron - altså en betapartikel - og omdanner stoffet til et stof, der er tungere jævnfør Tritium ovenfor.
I den høje ende af det periodiske system, er der oftest alfastråling.
Stoffet Uran, som er nr. 92, har tre isotoper i naturen:
- En med 142 neutroner (dvs. protoner + neutroner) bliver i alt 234.
- En med 143 neutroner altså 235 (den der var i den ene atombombe, 0,71 % i naturen).
- Og en med 148 neutroner altså uran 238 (99,28 %), den almindeligst forekommende i naturen.
De er alle alfa-radioaktive, med halveringstider på henholdsvis 248.000 år, 710.000.000 år henholdsvis 4.498.000.000 år - altså nogenlunde som jordens alder.
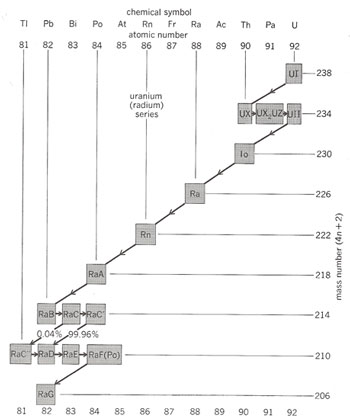
Alle tre er alfa-radioaktive, og udsendelsen af Heliumkernen ændrer dem til Thoriumisotoper (nr. 90), Uran 235 til isotopen med 141 neutroner. Dette er igen radioaktivt og henfalder, og sådan fortsætter det skiftende alfa- og beta-henfald med 12-14 henfald, endende med Bly nr. 82 med 125 neutroner.
Gamma-strålende stoffer findes stort set i hele det periodiske system, ofte fra stoffer som har undergået et af de andre henfald, og er endt med overskudsenergi i kernen, som den så skaffer sig af med ved et gamma-henfald uden kerneomdannelse. Disse henfald kan have fra meget små energier, til ret store energier.
På grund af halveringstiderne, er mange stoffer henfaldet, og stort set hel forsvundet igennem jordens 4,5 milliarder år, og de isotoper der er i naturen, er derfor fortrinsvis ikke radioaktive. De fleste radioaktive isotoper, er i den høje ende af det periodiske system.
En af undtagelserne er Kalium 40: 19 protoner og 21 neutroner, den er beta-radioaktiv med en halveringstid på 1,4*109 år, og findes naturligt i Kalium i 0,0119 %. Den indeholder vi alle, da vi ikke kan leve uden Kalium. Tilsvarende findes meget små mængder af en række andre radioaktive isotoper i vor krop.
Ovenfor blev ordet halveringstid brugt. Det er den tid der går, indtil halvdelen af kernerne i en klump kerner af samme isotop er henfaldet. Det viser sig, at henfaldet er en statistisk proces, dvs. at der er en bestemt chance for, at et atom af en given isotop henfalder i et bestemt tidsrum. Det betyder, at når man har mange atomer (og man har i små mængder stof som f.eks. et saltkorn i størrelsesordenen 1020 atomer) - omdannes der en bestemt brøkdel pr. tidsenhed.
Halveringstiden er den tid, som det tager halvdelen at blive omdannet. Den kan være fra brøkdele mikrosekunder, til længere end universets levetid.
Alle de henfald der er nævnt her, falder ind under gruppen spontane henfald - dvs. henfald der sker af sig selv, bare man venter længe nok. Det er altså det man kalder naturlig radioaktivitet.
Du kan finde mere på nettet i Wikipedia under: "Radioactive decays" eller på Google (på engelsk).
Med venlig hilsen
Malte Olsen
