Afkøling af sovs
Hejsa Spørg om Fysik
Jeg har i forbindelse med mit arbejde set en "Maskine" der kan køle sovs med vacuum.
 Sovsen er ca. 85 grader når det kommer i maskinen, og man bruger vacuum indtil 35 grader måles. Herefter er det så co2 man køler ned med...
Sovsen er ca. 85 grader når det kommer i maskinen, og man bruger vacuum indtil 35 grader måles. Herefter er det så co2 man køler ned med...
Jeg har søgt en del på nettet om der findes nogle formler for Nået Vacuum = maks. koge punkt. Jeg ved at der kan nås en vacuum ned til -0.90
Hvad er den mindste temperatur som maskinen kan opnå når vacuum'et er fjernet?
Med venlig Hilsen
K H

Den fysiske egenskab, der udnyttes i det du spørger om, er vands damptryk, så lad os i første omgang kun se på rent vand.
Pumper man al luft væk over en mængde rent vand og venter, vil der efter ligevægt indstille sig et tryk, som kun afhænger af temperaturen.
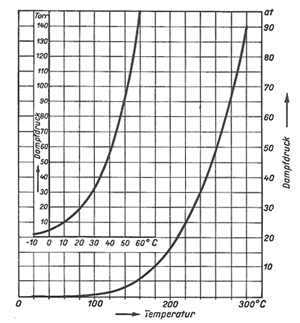 Se vedlagte graf fra Bergmann Schaefer:
Se vedlagte graf fra Bergmann Schaefer:
Den øverste graf viser vands damptryk fra 0 til 60 ⁰C og trykenhederne opad er i torr (efter Torricelli, Evangelista Torricelli 1608 - 1647) 1 torr er 1 mm Hg på et gammeldags kviksølvbarometer, det bliver 1/760 del af en atmosfære, som er det tryk, vi har i dagligdagen.
I dag bruges trykenheden Pascal (Pa), normaltrykket 1 atmosfære er 101 325 Pa, 1 Torr er 133,32237 Pa).
Den nederste graf viser det videre forløb, indtil kurven stopper ved det kritiske punkt, hvor der ikke er forskel på damp og væske. For vand ligger det ved 374,1 ⁰C og trykket 2,212 * 107 Pa (ca. 218 atm).
Trykket stiger kraftigt med temperaturen
Kurven viser, at trykket stiger kraftigt med temperaturen. Ser man på den nederste kurve, kan man se, at vands damptryk ved 100 ⁰C er 1 atmosfære. Det skyldes den måde vi definerer det normale kogepunktet af et stof. Det defineres, som den temperatur væsken har, når trykket er 1 atmosfære.
Er trykket lavere, f.eks. i bjerge, koger vand ved en lavere temperatur. Uanset hvor meget man varmer, kan man f.eks. ikke nå højere temperatur end f.eks. 85 ⁰C fordi den tilførte energi bruges til fordampning af vand. Derfor kan det tage lang tid at koge æg i bjergene.
Sænker man trykket over en vandmængde ved at udpumpe gassen f.eks. i en termobeholder med vand i bunden, vil vandet koge, fordampningen kræver energi og det fås ved afkøling af vandet.
Der vil hele tiden opnås ligevægt (hvis man venter et øjeblik) imellem trykket og vandets temperatur, som kurverne viser. Ser man på den øverste kurve, kan man se, at ved stuetemperatur dvs. 22 ⁰C er trykket ca. 20 torr eller 2666 Pa eller 0,026 atmosfære. Fortsættes pumpningen dannes is, som også har et damptryk, som afhænger af temperaturen, is kan altså fordampe selv om det går langsomt.
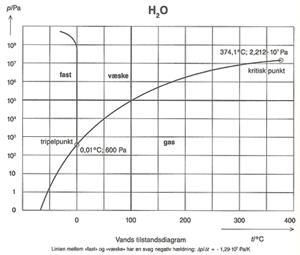 Næste billede fra Databog i Fysik og Kemi viser vands fasediagram, hvor man ser områder med is og damp, vand og damp og vand og is i balance, det er på kurverne. Tripelpunktet, hvor både damp fast stof og væske er i ligevægt ligger ved 0,01 ⁰C og 600 Pa, altså nær vands frysepunkt. Det bruges i specielt udformede celler til kalibrering af meget præcise termometre.
Næste billede fra Databog i Fysik og Kemi viser vands fasediagram, hvor man ser områder med is og damp, vand og damp og vand og is i balance, det er på kurverne. Tripelpunktet, hvor både damp fast stof og væske er i ligevægt ligger ved 0,01 ⁰C og 600 Pa, altså nær vands frysepunkt. Det bruges i specielt udformede celler til kalibrering af meget præcise termometre.
Med hensyn til sovsen, principielt kan man altså køle meget længere ned end 35 ⁰C, men da trykket bliver lavere og lavere går det langsommere og langsommere. Samtidigt sker der det, at man fjerner vanddamp, så sovsen bliver tykkere svarende til en indkogning, hvad man må tage hensyn til hvis man ønsker at bruge denne metode.
Skal man længere ned, har man som en mulighed et normalt køleskab eller dybfryser (som kan fås ned til temperaturer lavere end -65 ⁰C), som i brevet kulsyresne til ca. - 78 ⁰C, det er i øvrigt en ligevægt, imellem fast stof som fordamper og gas (i kulsyreslukkere er der væske i ligevægt med gas, ved højt tryk, det der kommer ud er faststof i ligevægt med gas).
Endeligt kan man bruge flydende nitrogen ved - 196 ⁰C. Det er en kogende væske i ligevægt med sin gas. Gør man som med vandet, kommer det i et termokar og pumper, falder temperaturen yderligere, indtil det bliver fast nitrogen.
Der findes pumper, som kan pumpe ned til tryk langt mindre end 1/1000 atmosfære, så det er ikke pumpen der stopper processen. Den bruges tværtimod i den proces der hedder frysetørring. Her fryses et produkt, trykket sænkes og isen sublimeres væk (fordamper direkte uden at blive til vand). Man anvender også tørringsprocesser f.eks. især tidligere på pulverkaffe, hvor kaffen sprøjtes ud vom væske i et tårn med lavt tryk, så væsken køles og fordamper. Derefter falder det tørre kaffepulver ned på bunden og opsamles. Vi har firmaer hjemme, som producerer sådanne industriapparater.
Jeg kan ikke let give dig en formel, tilnærmelsesformler findes, men damptrykskurverne kan give samme oplysning.
Med venlig hilsen
Malte Olsen
