
Er atomer og molekyler "udødelige"?
Kære brevkasse
Så vidt jeg har forstået (?), genbruges de samme nærmest udødelige molekyler i alt fysisk stof igen og igen helt fra urtiden og til nu.
Ifølge Bill Brysons "En kort historie om næsten alt" skulle nogle af nulevende menneskers molekyler således engang have siddet i helt andre dyr (inkl. krybdyr), planter, jord, hav, andre mennesker osv.
Er det samme enkelte molekyle da så "grundforms-agtigt", at det kan genbruges i hvadsomhelst på tværs af alle arter gennem jordens historie, og uanset om det er organisk eller uorganisk stof, de sidst har siddet i?
Venlig hilsen
Gitte Frederiksen

Svar:
Hej Gitte,
Det er i det store hele rigtigt, dog med nogle modifikationer:
Universet er bygget af af forskellige partikler. Nogle af disse partikler er selv bygget op af mindre partikler, mens nogle af dem er elementarpartikler, som — så vidt vi ved — er "fundamentale". Det vil sige, at de ikke kan brydes op i mindre bestanddele.
Den indskudte sætning "så vidt vi ved" bærer dog en tung byrde her, da fremtidige eksperimenter, som kan dykke dybere end vi er i stand til i dag, måske kan afsløre, at det vi tror er elementarpartikler, viser sig at være sammensat af noget mere fundamentalt.
Atomer og molekyler
Mennesker, dyr, planter, sten, cykelklokker og stjerner er alt sammen bygget op af atomer. Der findes lidt over 100 forskellige atomer, som f.eks. brint, kulstof, ilt, nitrogen, jern, guld, og uran.
Atomer består af en kompakt kerne, som er lavet af protoner og neutroner, som i sig selv er bygget op af noget der hedder kvarker. Det er antallet af protoner, som afgør hvilket slags atom vi har med at gøre. For eksempel har brint én proton, kul har seks protoner, osv. Typisk er der omtrent lige så mange neutroner, men det kan variere lidt.
Denne kompakte kerne er omgivet af en sky af elektroner. Hvor protoner er positivt ladede, er elektroner negativt ladede. Normalt er der lige så mange elektroner som protoner, men i visse situationer kan et atom mangle en eller flere elektroner, og somme tider kan de have for mange. Når der er sådan en ubalance mellem antallet af protoner og elektroner, må atomet overordnet set have en elektrisk ladning. Vi siger så, at atomet er ioniseret.
Elektronerne er (så vidt vi ved) elementarpartikler, og det er kvarkerne også.
Disse atomer kan forbinde sig i mere komplekse strukturer, som vi kalder molekyler. For eksempel består vand af vandmolekyler, som alle består af ét iltatom og to brintatomer. Ilten som vi indånder er ikke individuelle iltatomer, men ilt-molekyler, som består af to iltatomer. Når atomer sidder sammen i molekyler, deles de om nogle af elektronerne.
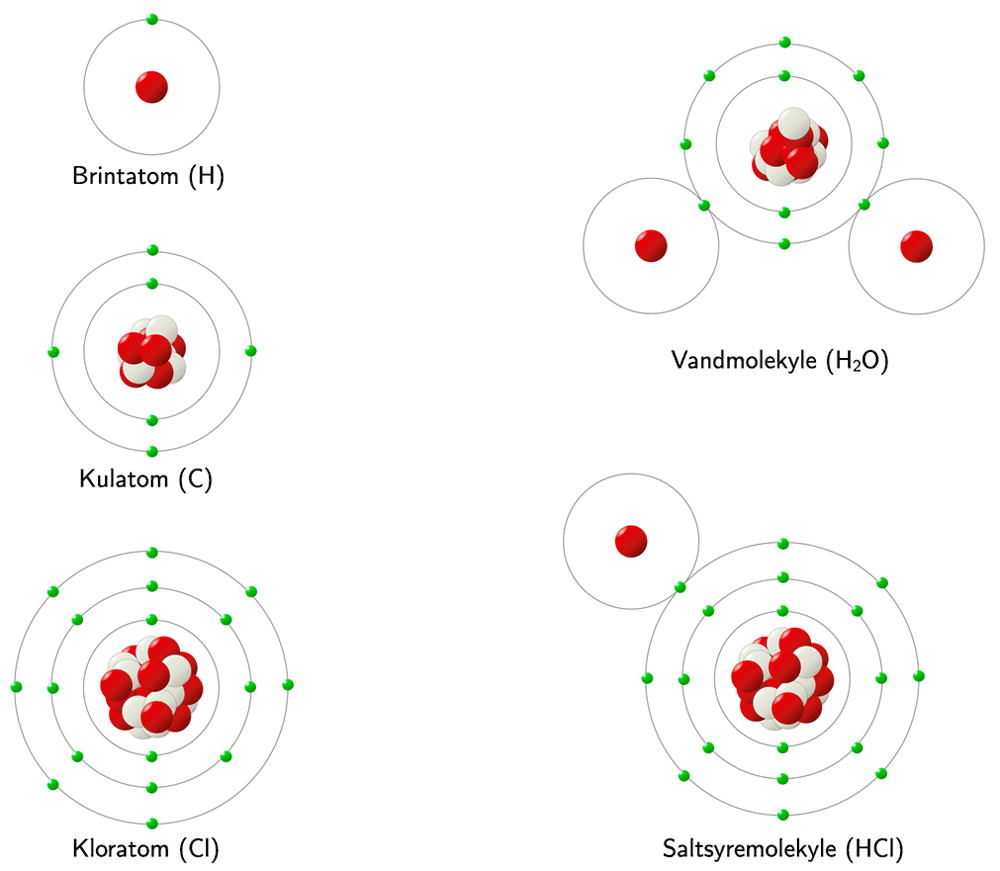
Eksempler på atomer (til venstre) og molekyler (til højre). Protoner er repræsenteret som røde kugler, neutroner som hvide, og elektroner som grønne. Denne repræsentation af partiklerne følger Niels Bohrs model fra 1913, som kan bruges til at forklare forskellige egenskaber ved atomerne. Men det er vigtigt at vide, at udover at modellen ikke er til skala overhovedet, og partiklerne ikke har farver, skal man heller ikke forestille sig, at elektronerne virkelig ligger i bestemte baner som planeter om en stjerne. Illustration: Peter Laursen.
Byggesten af byggesten
I figuren ovenfor kan du se, hvordan atomerne er bygget op, og hvordan de selv kan bygge molekyler op. Molekyler kan blive meget større og komplekse; f.eks. består molekylerne i stivelse typisk af 10.000 atomer, mens visse typer plastik består af molekyler med 100.000 atomer.
Det er dog ingenting imod vores DNA! I vores celler ligger 23 kromosom-par og svømmer rundt, og DNA'en i disse kromosomer er ét stort molekyle, som består af omtrent 100 milliarder atomer.

DNA-strenge er kendt for at være viklet op i en dobbelt-helix-struktur, som visualiseret her til venstre (kredit: Beckman Coulter), og fotograferet til højre (kredit Enzo Du Fabrizio / Francesco Gentile et al. 2012).
Lever partiklerne videre for evigt?
Så vores kroppe er altså bygget op at celler, som er bygget op af molekyler, som er bygget op af atomer, som er bygget op af elementarpartikler. Når vi dør, bliver vores kød og blod og celler nedbrudt. Ja faktisk sker det allerede inden vi dør, for de fleste af vores celler udskiftes hele tiden. Hudceller udskiftes efter nogle uger, mens f.eks. leverceller tager et års tid. Knoglecellerne holder omkring 10 år, og så er der nogle få slags, der holder hele livet.
Men selvom DNA'en nedbrydes, er der masser af molekyler, som ikke som sådan bliver nedbrudt. Halvfjerds procent af din krop består af vandmolekyler, som typisk ikke bliver nedbrudt, men forbliver det samme iltatom (O) og de samme to brintatomer (H), uanset hvilken celle det lå inden i, da det var en del af din krop, og uanset hvad der sker med den celle efterfølgende, om det så bliver nedbrudt af bakterier, fordamper og bliver til en sky, regner ned 1000 km væk, bliver drukket af et får, som senere bliver spist af et andet menneske og indgår i opbygningen af dette menneskes krop.
Der er processer, der ind imellem nedbryder vandmolekyler, men i de tilfælde kan de tre atomer så indgå i nye kemiske forbindelser. Så lige som et Lego-hus kan skilles ad og bygges om til en Lego-bil, af de samme grundliggende Legoklodser, så kan molekylerne splittes ad og samles til nye molekyler.
I molekylerne deles atomerne dog om nogle af elektronerne, så f.eks. et iltatom som indgår i et vandmolekyle, og senere indgår i et fedtmolekyle, kan få udskiftet nogle af sine elektroner. Så om man vil kalde det præcis det samme atom, eller om man vil kalde det en modificeret udgave, er lidt et definitionsspørgsmål. Og så alligevel: Atomer beskrives med den gren af fysikken, som kaldes kvantemekanik, og ifølge den er alle elektroner 100% ens. Der er ingen forskel overhovedet, hvis du bytter om på to elektroner. Det er udenfor rammerne af dette svar at gå dybere ind i dette fænomen, men det betyder, at du godt kan sige, at et atom er "udødeligt".
Kernekræfter
Selv dette udsagn har dog dét aber dabei, at et tungt atom i princippet kan blive splittet ad i to lettere atomer. Denne proces involverer kernekræfter, som er langt stærkere end de kemiske kræfter, vi har snakket om indtil videre, og typisk har at gøre med atomkraftværker, stjerneeksplosioner og sådan noget.
Nogle atomer kan dog spontant splitte sig selv ad — de er radioaktive. De fleste atomer i kroppen er ret stabile, men en lille andel af vores kulatomer har et par ekstra neutroner, hvilket gør dem ustabile. En sjælden gang i mellem kan én af disse ekstra neutroner lave sig selv om til en proton og en elektron, hvorved kulatomer bliver til et nitrogenatom. Man udnytter dette til at se, hvor mange år siden det er, at noget organisk stof døde, f.eks. et mosefund, træet i et vikingeskib, eller et papyrus-ark. I disse sjældne tilfælde kan man altså sige, at et atom ikke længere er det samme atom.
Så på en måde lever du videre — ikke bare i minderne hos dem, der kendte dig — men i vandmolekylerne i en regndråbe, i kulatomerne i et træ, eller i luften, som et andet menneske en dag indånder. Universets byggesten går ikke tabt — de skifter bare form og rejser videre.
Bedste hilsener,
Peter Laursen, Astrofysiker og videnskabsformidler
Cosmic Dawn Center, Niels Bohr Institutet.
